广州科适特科学仪器有限公司代理商
10 年
手机商铺
- NaN
- 0.3999999999999999
- 1.4
- 0.3999999999999999
- 3.4
推荐产品
公司新闻/正文
如何对心血管系统中的内皮细胞进行体外研究
510 人阅读发布时间:2024-07-24 09:26
血管生成中的内皮细胞
血管生成是新血管的生长过程。因此,它在发育生物学、伤口愈合和肿瘤生长中都发挥着作用(见图 1)。血管生成本身由多个步骤组成,包括:
- 血管内皮细胞增殖
- 定向迁移(通常通过趋化作用进行)
- 管形成及管腔化
- 成熟:融合、重塑、募集辅助细胞(如周细胞和血管平滑肌细胞)
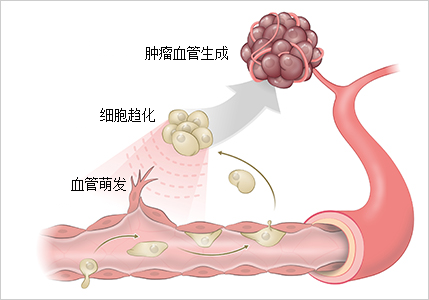
上述步骤协同作用于血管生成的整个过程之中,即新血管由既有血管发展而来。血管生成过程的复杂性不言而喻,为了全面解析这一机制,研究者需深入探究其各个构成要素。通过体外实验方法,实验者能够聚焦于血管生成特定环节的细致研究,从而实现更为精确、可控及详尽的分析。
研究案例 1:探究间隙连接在内皮细胞迁移中的作用
Mannell 等人在 2021 年的研究中探究了间隙连接蛋白 43( Connexin 43,Cx43)在血管内皮细胞迁移和血管生成中的作用。研究团队发现,若用 siRNA 对人微血管内皮细胞(Human Microvascular Endothelial Cells, HMECs)中的 Cx43 基因进行敲低处理,则细胞的迁移能力显著减弱(如图 2 所示)。在探讨其潜在机制时,研究团队揭示了 Cx43 的功能是通过与 Src 同源 2 结构域蛋白酪氨酸磷酸酶(Src Homology 2 Domaincontaining Protein Tyrosine Phosphatase,SHP 2)之间的相互作用介导的,从而影响了细胞迁移的生物学过程。
为了研究 CX43 在心肌细胞迁移中的作用,研究人员在 ibidi µ-Slide 8 孔腔室载玻片中放置了 ibidi 细胞划痕插件,以评估细胞的迁移速率和方向性。
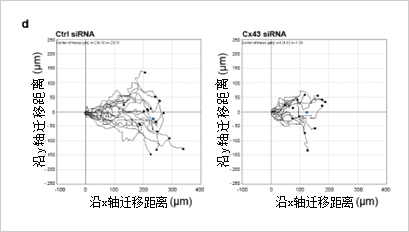
研究结果明确指出,内皮细胞的迁移与血管生成过程依赖于 Cx43 的参与,且这一作用机制是通过 SHP-2 的介导实现的。
屏障生成中的内皮细胞
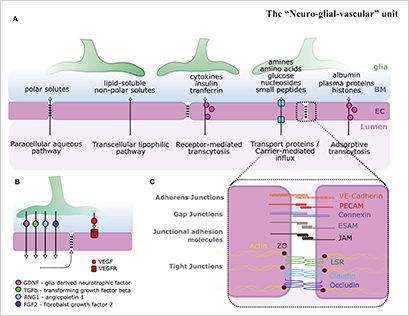
血管内的单层内皮细胞在血液与周围组织间构筑了一道至关重要的屏障,尤其以血脑屏障(Blood-Brain Barrier, BBB)最为人所熟知。这些细胞通过调控多种转运途径——包括细胞旁途径的水性扩散、跨细胞途径的亲脂性转运、受体介导的主动转运、载体介导的转运以及非特异性的吸附性转运(如图 3 所示)——以调节各类物质的跨膜转运。
鉴于内皮细胞屏障在药物递送、药理学、毒理学以及肿瘤学研究中的重要地位,深入探究其功能特性与分子机制已成为科研界广泛重视的热点领域。
研究案例 2:建立血脑屏障体外模型
Choublier 等人在 2021 年发表的研究中,深入剖析了研究血脑屏障时所遭遇的实验性挑战。鉴于血脑屏障的特殊位置——深藏于大脑内部,以及其对恒定、层流、均匀血流条件的严格要求,这一研究领域确实存在显著难度。为克服这些障碍,研究人员设计并构建了一种既坚固耐用又成本低廉的实验装置。该装置通过将上部通道与 ibidi 流体剪切力系统相连接,实现了培养基的单向再循环,持续时间长达 4 天,从而高度模拟了生理条件下的血脑屏障环境。
Choublier 团队的研究进一步证实,该装置在评估血脑屏障功能(如图 4 所示)及研究药物跨血脑屏障转运机制方面展现出了极高的应用价值。此外,利用 ibidi 流体剪切力系统与 ibidi µ-Slide 通道载玻片,研究者们还能够有效评估并复制人类肠道或肾脏等细胞类型中的屏障特性,进一步拓宽了研究范围。
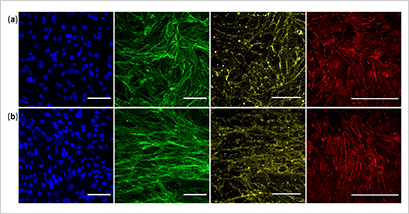
尤为值得一提的是,构建一个能够精确调控流量的系统,为在更接近体内环境的条件下研究心肌细胞提供了可能。相较于静态系统,此类动态系统能够更准确地模拟真实的生理状况,为生物医学研究带来了革命性的进展。
灌流培养下的内皮细胞
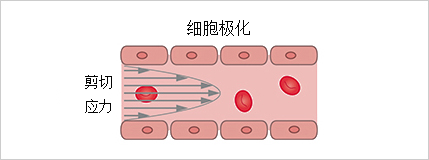
流体环境中产生的剪切应力对心肌细胞的电生理极化状态、蛋白质表达谱以及细胞形态结构具有显著的直接影响(如图 5 所示)。当前研究聚焦于两大方向:一是深入探索静态流体条件对生理状态下内皮细胞功能调控的具体机制;二是分析扰动流体动力学机制在动脉粥样硬化等病理过程中的作用与影响。
研究案例 3:探究线粒体在心肌健康中的作用
Hong 等人在 2022 年开展的研究深入探究了线粒体在维系心血管稳态与健康中的核心作用。该研究发现,在血流受扰动的区域,线粒体碎片化的现象显著增强,而在血流单向顺畅的区域,线粒体则主要呈现伸长状态。这一发现揭示了血流模式对线粒体融合与分裂动态过程的深刻调控作用,进而影响心血管细胞的炎症响应及代谢状态。为探究这些流动依赖性动力学机制,研究人员采用了 ibidi 流体剪切力系统进行了实验分析。
综上所述,该研究揭示血流状况对心血管细胞健康有至关重要的影响,且这一影响在一定程度上是通过线粒体形态与功能的适应性变化所介导的。
炎症中的内皮细胞
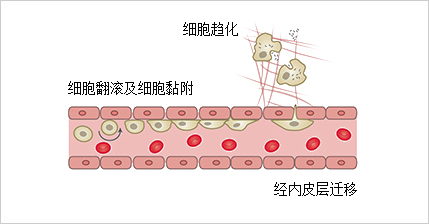
全身性炎症反应对心血管细胞及其与其他细胞间的相互作用产生直接影响。具体而言,心血管细胞所构成的屏障功能在炎症环境下趋于减弱,表现为屏障通透性增加。同时,免疫细胞的行为,包括细胞滚动、趋化迁移以及跨内皮层迁移等过程,均在炎症过程中显著加剧,从而进一步促进了炎症反应的扩展与深化(如图 6 所示)。
研究案例 4:探究动脉粥样硬化诱因
Forde 等人于 2020 年开展的一项研究深入探讨了肿瘤坏死因子相关凋亡诱导配体(TNF-related Apoptosis-inducing Ligand,TRAIL)在模拟促动脉粥样硬化条件下对人主动脉内皮细胞(Human Aortic Endothelial Cells,HAECs)的具体作用机制。研究发现,在受到振荡剪切应力作用的 HAECs 中,TRAIL 能够诱导细胞基因表达模式向抗氧化方向转变,从而展现出显著的血管保护效应。进一步地,当 HAECs 同时暴露于 TNF-α 和高血糖环境下时,TRAIL 有效减少了活性氧(Reactive Oxygen Species,ROS)的生成。上述发现支持了 TRAIL 通过缓解氧化应激来保护动脉内皮细胞的观点。
本研究联用了 ibidi 流体剪切力系统与 ibidi 通道载玻片,构建了一个高度模拟动脉粥样硬化病理过程中振荡剪切应力的体外培养模型。该模型已被广泛认可为能有效促进动脉粥样斑块形成特征的重现,为本研究提供了坚实且先进的实验平台。