广州科适特科学仪器有限公司代理商
10 年
手机商铺
- NaN
- 0.3999999999999999
- 1.4
- 0.3999999999999999
- 3.4
推荐产品
公司新闻/正文
选择活细胞成像的 5 大理由
377 人阅读发布时间:2024-07-16 09:28
在进行活细胞成像时,实验者需审慎考虑一系列挑战与要求。首要的是,确保显微镜系统配备有载物台培养箱,该培养箱能够模拟并维持适宜的环境条件,对于细胞的长时间存活、活力保持及健康状态至关重要。
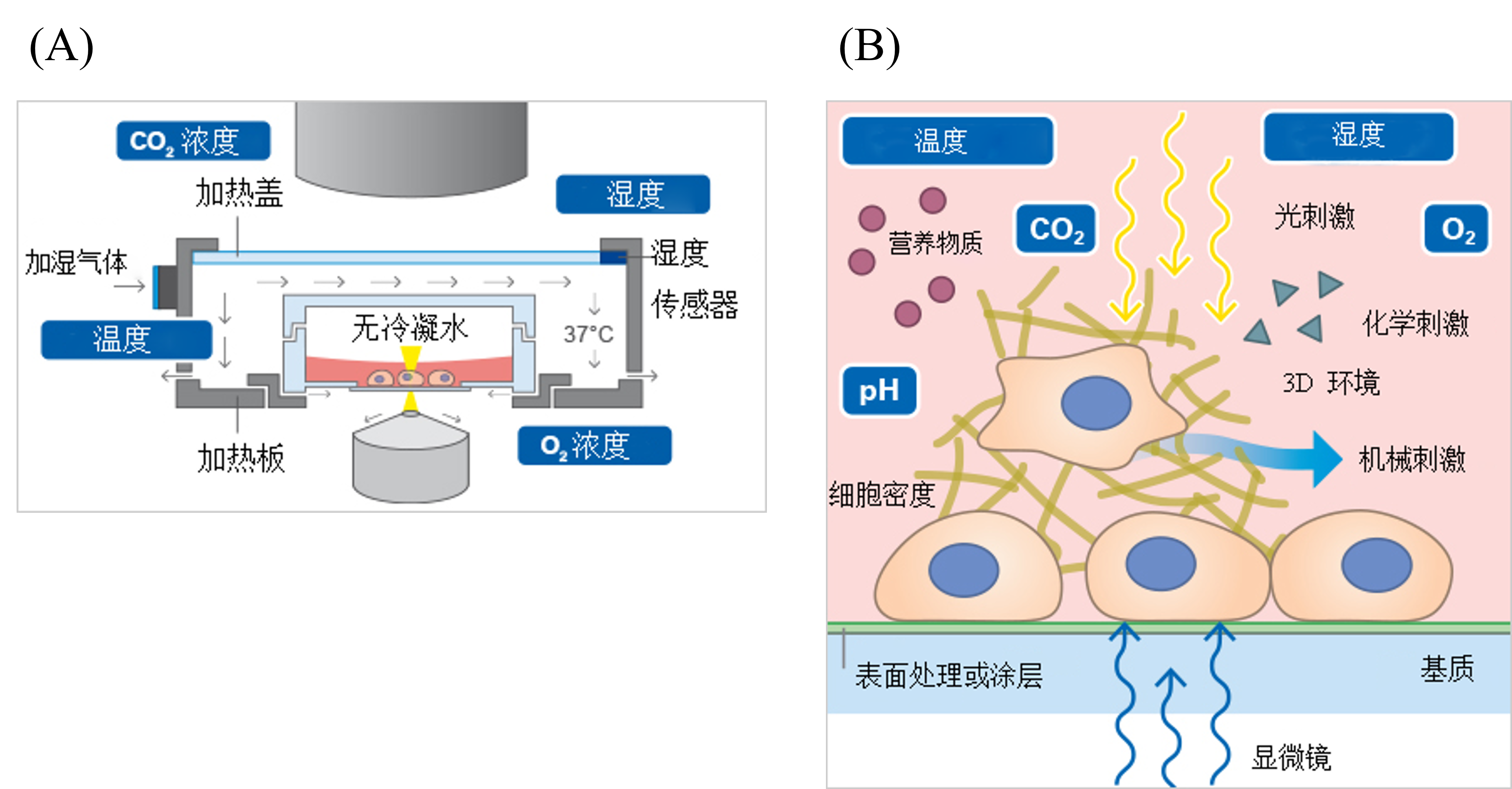
图 1:(A)活细胞成像过程中需要考虑和控制的环境参数;(B)倒置显微镜载物台培养箱示意图。
既然基础知识已阐述完毕,接下来我们可以直接探讨为何采用活细胞成像技术来研究细胞的深层次原因:
避免细胞固定造成的伪影
在显微镜镜检,尤其是免疫荧光等实验中,细胞通常需要经过固定处理以维持其形态稳定。多年来,为了优化原始样本的保存质量,多种化学与物理固定方法已被广泛研究与确立。
然而,固定过程本质上是一种不可逆的细胞损伤手段,它导致细胞死亡,并显著改变细胞的组织结构、形态学特征(如细胞器萎缩、蛋白质分布异常等)。相较之下,活细胞成像技术则允许我们直接观测和研究处于自然状态下的活细胞,这些细胞能够展现其固有的生理活动与行为模式。尽管活细胞成像过程中可能会受到荧光标记、激光照射等外部因素的干扰,但这些因素可通过适当的环境条件控制来最小化其影响。
观察和分析细胞动态过程
活细胞成像技术为实验者提供了一个强大的平台,用于监测细胞群体、单个细胞乃至亚细胞层面的动态变化。与固定细胞相比,后者仅能捕获细胞在某一特定时间点的静态状态,而活细胞显微镜则能够连续追踪并记录细胞在动态过程中的行为变化。这一技术特别适用于基于细胞功能的研究,如细胞划痕(如图 2 所示)以及细胞趋化实验等,这些实验能够深入探究细胞在化学(如细胞趋化实验)或物理(如细胞划痕实验)刺激作用下的行为。
实时追踪细胞动态变化
活细胞显微镜作为一种至关重要的技术手段,能够实时且连续地监测细胞的时空演变过程,从而避免了仅依赖于固定细胞样本进行终点分析的局限性。
借助延时视频显微镜,实验者能够对细胞进行长时间、高精度的跟踪观察,进而捕获到一系列细胞内部发生的动态结构重排现象,如细胞在趋化信号刺激下展现的骨架极化过程(如图 3 所示),或是细胞有丝分裂期间染色体分离的瞬时事件。相比之下,固定细胞方法则无法捕捉这些关键的动态变化过程。
研究单分子动力学、定位及相互作用
随着光漂白后荧光恢复术(Fluorescence Recovery After Photobleaching,FRAP)、荧光寿命显微成像术(Fluorescence Lifetime Imaging,FLIM)及荧光共振能量转移( Fluorescence Resonance Energy Transfer,FRET)等先进荧光标记与成像技术的不断发展,科学家们现已能够在活细胞成像的框架内,精准地观察并分析单分子的定位、动力学特征及其相互作用。
具体而言,FRAP 技术被广泛应用于量化活细胞内荧光标记分子与蛋白质的流动性;而FLIM技术则通过测量附着荧光团的寿命,揭示了细胞分子分布及其所处微环境的深层次信息。此外,FRET 作为一种强有力的工具,允许科学家通过监测纳米尺度上两个分子间荧光团的相互作用,直接测量活细胞内两个分子间的直接相互作用,为理解细胞内部复杂网络提供了全新的视角。
从单次实验中最大化信息获取
总体而言,采用活细胞成像技术相较于固定细胞成像,能够显著地提升单次实验中的信息获取量。这是由于活细胞成像技术能够实时追踪分子动力学及其动态变化,从而为我们所关注的细胞过程构建出一个更为广阔且详尽的视图。
相比之下,对固定样本的分析通常仅能提供细胞事件某一瞬间的静态快照,而通过对整个动态过程的连续跟踪,我们能够测量更多维度的参数,进而从单次实验中推导出更为丰富且多样的结论。