广州科适特科学仪器有限公司代理商
10 年
手机商铺
- NaN
- 0.3999999999999999
- 1.4
- 0.3999999999999999
- 3.4
推荐产品
公司新闻/正文
3D 细胞培养:显微镜下的艺术与科学之美
641 人阅读发布时间:2024-07-09 15:08
小鼠小肠类器官
图 1 生动展示了小鼠小肠 organoid 的三维培养体系,其核心目的在于评估 IL-22 细胞因子对肠道内抗菌蛋白表达的影响,特别是聚焦于抵抗素样分子 β (resistin-like molecule beta,RELM β)的表达情况。实验过程中,类器官置于预热的 ibidi µ-Slide 8 孔高壁载玻片中并嵌入 Matrigel® 基质胶中进行培养,随后进行免疫荧光染色处理,所使用的染料如下所示:
- 抵抗素样分子 β:抗抵抗素样分子 β 抗体(绿色)
- 分泌细胞标志物:荆豆凝集素 I(Ulex Europaeus Agglutinin I,UEA I,红色)
- β-连环蛋白:抗 β-连环蛋白抗体(紫色)
- 细胞核:DAPI(蓝色)
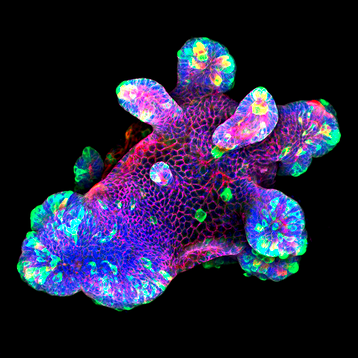
图 1:小鼠小肠类器官
成像采用了蔡司 LSM 880 共聚焦显微镜,配备 20 倍物镜,确保了高分辨率的图像捕获。本研究通过高度模拟体内肠上皮细胞的微环境,为深入探究 IL-22 对抗菌肽表达调控的机制,以及免疫细胞释放的细胞因子与肠上皮细胞间复杂交互作用,提供了极具价值的实验证据和理论支持。
人乳腺癌类器官
图 2 呈现了从患者肿瘤活检组织中成功培育的人类乳腺癌类器官的复杂结构。本研究的核心目标在于构建类器官内部的肿瘤微环境,以高度模拟药物与肿瘤细胞的相互作用,进而推动个性化治疗策略的发展。
获取肿瘤样本后,实验者随即进行解剖与酶解处理,以确保细胞的完整释放。随后,将预处理后的组织植入 Matrigel 基质胶中培养,随后进行免疫荧光处理。免疫荧光染色所使用的染料如下所示:
- 细胞增殖标志物:抗 Ki67 抗体(品红色)
- 细胞骨架:抗 F-肌动蛋白抗体(绿色)
- 细胞核:DAPI(蓝色)
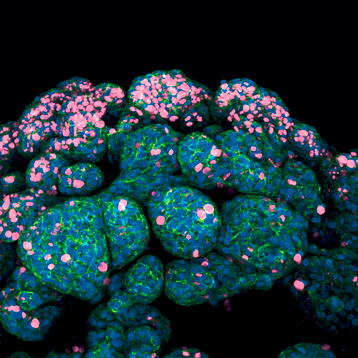
图 2:人乳腺癌类器官
所得 organoid 在 35 mm 高壁玻璃底部 µ-Dish培养皿中进行培养,并用 ANDOR Dragonfly 高速共聚焦显微镜系统搭配 25 倍物镜进行成像。
小鼠胚胎干细胞三维聚集体(gastruloids)
图 3 展示了小鼠胚胎干细胞在轴伸展前阶段形成的三维聚集体(gastruloids),该模型模拟了胚胎发育过程中生殖细胞与多能细胞的自然分离过程。本研究聚焦于细胞命运的空间组织模式及其对邻近细胞的潜在影响,深入分析了三维组织结构及单细胞层面的动态变化。
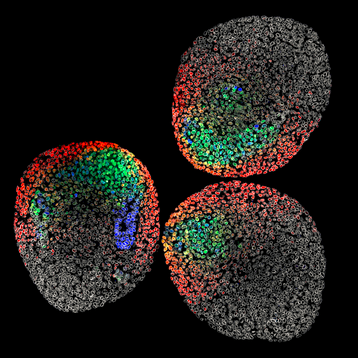
图 3:小鼠胚胎干细胞三维聚集体
样品制备过程中,研究者运用了基因标记技术,通过特异性标记 Sox2 (标记为蓝色)、Brachyury(T,标记为绿色)、Tbx6(红色)及 LaminB1(灰色)等转录因子,揭示了上述转录因子在神经中胚层前体细胞(NMPs)中的空间分布及分化时序。随后,实验者用水:甲醇稀释液对样品进行梯度脱水使其透明化(即 BABB 透明化法),以优化深层组织的光学成像效果。
图 3 由徕卡 Sp8 共聚焦显微镜捕获,并采用 40 倍油浸物镜结合徕卡 LIGHTNING 系统,在 ibidi µ-Slide 8 孔高壁载玻片上进行拍摄。此图像直观地呈现了细胞命运模式的精细图谱及整体胃肠形态的结构特征,为深入理解胚胎发育机制提供了宝贵的图像资料。
小鼠回肠类器官
图 4 展示的是在载有 Matrigel® 基质胶的 ibidi µ-Slide 8 孔高壁载玻片中培养的小鼠回肠类器官。该研究旨在分析宿主与病原体(尤其是人类限制性病原体)之间的相互作用。采用三维类器官成像技术可深入研究相关病原体在复杂组织微环境中的入侵机制及其细胞内生存策略。为细致观察类器官结构,所采用染色方案如下:
- F-肌动蛋白:鬼笔环肽(绿色)
- 细胞质膜:CellMask(红色)
- 细胞核:DAPI(蓝色)
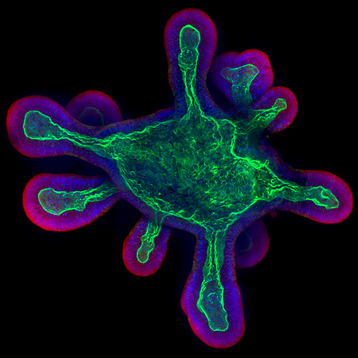
图 4:小鼠回肠类器官
染色后,实验者使用 Zeiss Cell Observer 共聚焦显微镜以 40 倍物镜进行成像。为了达到合理的分辨率和成像深度,将 organoid 接种在预冷的 ibidi μ-Slide 8 孔高壁载玻片上,以防止 Matrigel 基质胶凝固,确保它们沉降在盖玻片底部附近,以优化图像分辨率。
人肠道成纤维细胞及内皮细胞球状体
图 5 展示了在纤维蛋白基质胶中构建的,集成了人类肠成纤维细胞与内皮细胞的复合细胞球状体模型。本研究的核心聚焦于探索肠道细胞球体内部血管生成的策略。此模型被称为「血管化单元」(Vascularization Units, VUs),其特色在于将人内皮祖细胞与肠成纤维细胞共同培养,并嵌入到 ibidi µ-Slide 4 孔腔室载玻片上的纤维蛋白基质胶中培养 3 d,以模拟体内血管化过程。

图 5:人肠道成纤维细胞及内皮细胞球状体
所采用的染色及成像方案如下:
- 内皮细胞:抗 CD31 抗体(黄色)
- 成纤维细胞:抗波形蛋白抗体(红色)
- 细胞核:DAPI(蓝色)
- 使用 Leica TCS SP5 II 共聚焦显微镜和 10 倍物镜进行成像
实验过程中不难观察到一个关键现象:成纤维细胞的过度增殖显著阻碍了球状体内血管网络的正常构建过程。为应对此挑战,实验者需要在凝胶固化过程中将载玻片上下倒置。此举有效规避了球状体因重力作用而沉降并贴附于培养孔底部的问题,进而促进了血管生成的效率与质量,为整体研究成果的提升奠定了坚实基础。