广州科适特科学仪器有限公司代理商
10 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.3999999999999999
- 1.4
- 0.3999999999999999
- 3.4
可视细胞趋化实验服务
询价
推荐产品
公司新闻/正文
HT-1080 细胞的二维及三维细胞趋化实验步骤全解析
826 人阅读发布时间:2024-06-24 10:47
实验材料
活细胞成像装置是进行细胞趋化迁移研究的基础条件。为了实现高效且全面的观察,建议使用电动平台和自动对焦(x、y、z)设备,用以平行观察同一张载玻片上的所有 3 个腔室乃至多片载玻片。有关实验所需硬件和软件配置的详细信息,请参阅以下应用指南:
在二维和三维细胞趋化实验中,本指南均采用 µ-Slide 3D 细胞趋化载玻片(ibidi,80322)作为实验平台。对于三维实验环境的构建,本指南通过将 HT-1080 人纤维肉瘤细胞嵌入胶原蛋白 I 基质胶或 Matrigel 基质胶来实现。关于胶原蛋白 I 基质胶的制备,所需的全部成分清单及详细的操作步骤详见以下应用指南:
此外,本实验所需的 30% Matrigel 基质胶的具体组分请参阅「重要实验参数」一节中的表 2。关于 Matrigel 基质胶的使用和处理,建议参考生产商提供的相关指引。
实验步骤
1)重要实验参数
α. 二维细胞趋化实验参数(仅供参考)
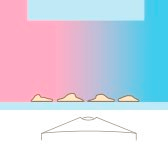
图 1:二维细胞趋化实验
-
细胞类型: HT-1080 人纤维肉瘤细胞
-
细胞培养基:DMEM 培养基(含 10% 胎牛血清)
-
细胞培养表面:ibiTreat
-
最终细胞密度:
-
趋化诱导剂:10% 胎牛血清
-
延时摄像时间间隔: 24 h 内每 10 min 1 次
-
物镜倍率:4X(使用相差显微镜镜检)
按标准操作流程制备细胞悬液,并调整到所需细胞密度。用移液器将细胞悬液加入载玻片通道,使细胞贴壁。在储液池中加入培养基和趋化诱导剂后,立刻开始延时摄像。
β. 三维细胞趋化实验参数(仅供参考)

图 2:三维细胞趋化实验
-
细胞类型: HT-1080 人纤维肉瘤细胞
-
细胞培养基:DMEM 培养基(含 10% 胎牛血清)
-
细胞培养表面:ibiTreat
-
最终细胞密度:
-
趋化诱导剂:10% 胎牛血清
-
基质胶:牛源、大鼠尾源胶原蛋白 I 基质胶
-
延时摄像时间间隔: 24 h 内每 10 min 1 次
-
物镜倍率:4X(使用相差显微镜镜检)
按照标准流程制备细胞悬液,并调整到所需细胞密度。随后,将细胞悬液与胶原蛋白充分混匀,并将混合液加入载玻片通道。待凝胶化完全且填充储液池完毕后,将载玻片置于显微镜下,开始延时摄像。
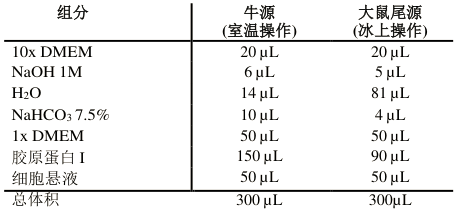
表 1:1.5 mg/mL 牛源、大鼠尾源胶原蛋白 I 基质胶的组分,所有组分按移液顺序排列
2)设置对照
实验设计不仅包括趋化处理组(+/-)本身,还包括两个对照组(+/+、-/-)。两个对照组对应的处理是在腔室中仅加入趋化诱导剂溶液(+)或不含趋化诱导剂的培养基(-)。这些对照实验有助于确定给定物质是否会影响细胞的定向移动和/或随机迁移。
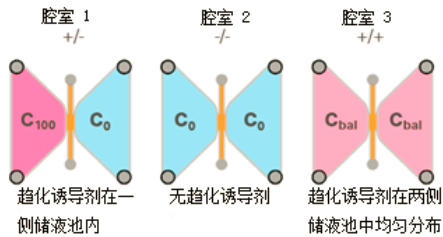
图 3:针对单片细胞趋化载玻片的推荐实验设计
应用示例: 使用 10% 胎牛血清作为趋化诱导剂的二维、三维细胞趋化实验比较
细胞的迁移行为受细胞环境及所使用的趋化诱导剂的影响。以下示例数据详细描述了在不同培养条件下,人类脐静脉内皮细胞(HUVEC)迁移行为的差异,培养条件包括:
-
在二维表面上(ibiTreat)直接培养;
-
包埋于大鼠尾源或牛源胶原蛋白(浓度为 1.5 mg/mL)基质胶中培养。
在所有上述培养条件下,本示例均使用 10% 胎牛血清(FCS)作为趋化诱导剂。
为了准确评估细胞迁移行为,并确保数据的均一性,细胞迁移分析在 6 h~18 h 时间段内进行。这同时避免了因长时间培养可能导致的营养匮乏对细胞行为的影响。
如果符合以下标准并具有统计学相关性,则认为实验表现了趋化作用:
+/- 实验组:
- FMI//>FMI⊥
-
Rayleigh 检验 p<0.05
+/+、-/- 对照组:
- FMI⊥≈0 且 FMI//≈0
-
Rayleigh 检验 p>0.05
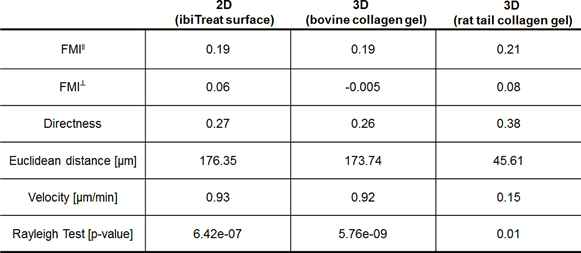
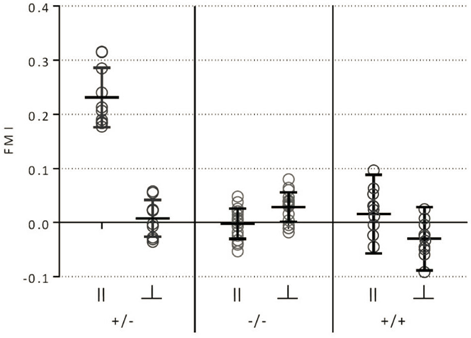
在所有设定的培养条件下,均能明确观察到细胞的趋化反应。通过趋化实验所得的 和 Rayleigh 检验 p 值均显著指示细胞呈定向迁移。然而,在分析迁移参数时,不难发现细胞的欧氏距离(Euclidean distance)和迁移速率(Velocity)存在显著差异。具体而言,在二维表面培养的细胞,其平均欧氏距离达到 176 μm,而平均迁移速率则为 0.9 μm/min;将细胞包埋于浓度为 1.5 mg/mL 牛源胶原蛋白 I 基质胶中进行培养,同样可以观察到与在二维表面培养时相类似的迁移特征;相比之下,若将细胞包埋于浓度为 1.5 mg/mL 大鼠尾源胶原蛋白 I 基质胶中进行培养,其迁移速度显著减缓,平均覆盖距离缩减至 45 μm。