广州科适特科学仪器有限公司代理商
10 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.3999999999999999
- 1.4
- 0.3999999999999999
- 3.4
血管生成实验服务
询价
推荐产品
公司新闻/正文
血管生成实验的数据分析
1163 人阅读发布时间:2024-06-13 10:04
血管生成实验是评估物质对培养细胞抗或促血管生成作用的有效工具。通过对比物质处理后的细胞与对照细胞培养物,可以利用血管长度和在 Matrigel 基质胶表面形成的环数量等参数来量化物质的影响。
请注意:术语「血管」用于描述在已形成的网络中可见的细胞束,这并不代表这些细胞束具有内部腔道。
为确保血管生成实验的准确性,需优化实验方案并建立可靠的数据采集方法。实验设置中的关键要素包括数据采集的时间点、细胞接种密度以及细胞培养基中的血清浓度。
本应用指南旨在协助优化利用您自身细胞系进行的血管生成实验设计,确保数据收集的可靠性和实验结果的重复性。
在本应用指南的部分内容中,我们提及了 ibidi µ-Slide 3D 96 孔板,但请注意,在任何培养容器中进行的血管生成实验都将呈现相似的特性,且数据处理方式也相同。
确立培养体系
开展血管生成实验的首要步骤是确立培养体系。在选择时,需着重考虑以下三个核心要素:
-
细胞类型:鉴于血管生成主要在内皮细胞中观测到,因此需慎重选择内皮细胞。
-
基质胶:必须确保其与所选细胞类型相容,并能为细胞贴壁提供必要的结合基团。
-
培养基组成:需评估是否需要添加生长因子以促进细胞生长。
对于大多数内皮细胞而言,推荐的培养体系应包括 Matrigel 基质胶、低生长因子培养基,以及含有 2% 或更低血清浓度的内皮细胞培养基。这样的培养条件能够满足大多数内皮细胞的生长需求,并为血管生成实验提供稳定的细胞环境。
数据分析综述
为了深入理解方案优化的后续步骤,我们需要对数据分析参数进行系统性概述。
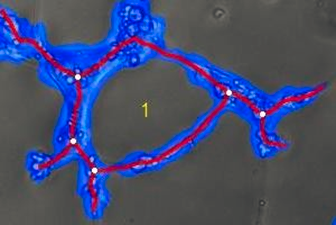
如图所呈现的显微图像,详细展示了管形成网络,其中包含四个关键的量化指标:
-
细胞覆盖面积(以蓝色标示)
-
管状结构(以红色标示)
-
环形结构(以黄色标示)
-
分支点(以白色标示)
基于这些基础指标,可以进一步计算得出更多衍生指标,例如平均管长、总管长以及环路的平均面积。
对于图像分析,存在多种科学方法。一种常见的方法是采用图像处理软件(如 ImageJ 的「AngioTool」插件)进行手动分析;另一种则是利用 ACAS 等自动图像分析平台实现自动化分析。
实验前准备
在进行实验之前,优化实验设计是不可或缺的步骤。
1)优化实验设计
细胞接种密度、数据采集时间点和血清浓度对数据结果具有显著影响。因此,制定详尽且严格的实验方案对于确保数据的可重复性和数据集间的可比性至关重要。
α. 确定测量时间间隔
首先,需选择合适的细胞浓度和促进血管生成的条件,以记录时间曲线。对于每孔约 10,000 个人脐静脉内皮细胞(HUVEC),使用含低量生长因子的 Matrigel 基质胶和不含血清或生长因子的细胞培养基即可。
随后,按照以下应用指南中的相关指引,制备基质胶和细胞悬液。细胞接种至基质胶表面后,应立即将载玻片置于载物台培养室内,并开始延时录像。每 10 min 捕获一次图像,并在每个时间点使用软件工具调整焦距。若显微镜不具备培养室,则在最初的 8~10 h 内,至少每 1 h 捕获一次图像。每次录像后,应立即将样品放回细胞培养箱中。过夜培养后,记录最终图像。
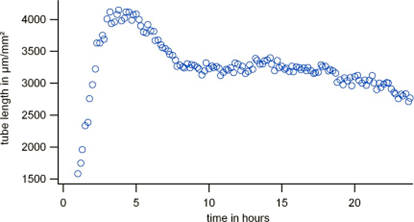
最终,运用专业的软件对图像进行分析,并将关键参数(如血管总长)的随时间变化曲线进行可视化处理。通常,该曲线首先呈现上升趋势直至达到最大值(约 0~5 h),随后进入一个相对稳定的阶段(从约 7 h 时开始),并最终趋于平缓(超过 20 h 时)。鉴于所有四个关键参数在特性上展现出相似的变化趋势,评估其中一个参数即可代表整体情况。我们选择了血管总长作为评估参数,因为其原始图像提供了一个基准,便于与后续评估的图像进行直接比较。
最佳结果通常出现在达到最大值的阶段,以及随后稳定且未出现急剧下降的阶段。在上图中,4 h 和 10 h 的时间点往往被视为理想的测量参考时间点。
β. 确定细胞接种密度
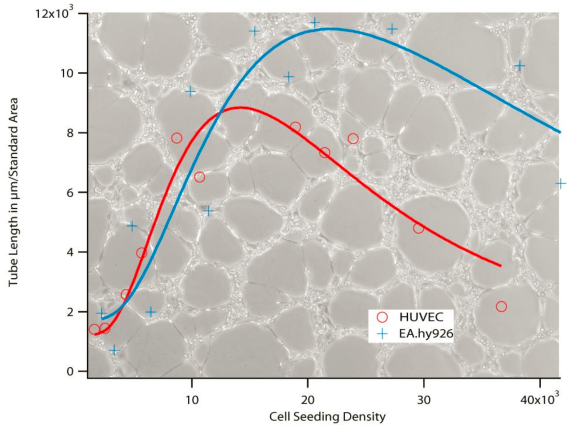
为了确定细胞接种的最佳密度,需要记录并分析细胞系的特性。
首先,在 范围内对细胞进行稀释,随后将稀释后的细胞接种至基质胶表面。按照第(1)-α 节的相关指引,将接种后的样品孵育至预设时长,并使用相差显微镜获取镜检图像。每个细胞浓度均进行五次独立的平行实验,以确保结果的准确性。
图像分析遵循「数据分析综述」以及「数据分析」两节中所述的方法。随后,将收集的数据绘制成图表,以直观地展示结果。数据图表将呈现一条特征曲线,该曲线具有一个明显的最大值点。此最大值点对应的细胞浓度即为该细胞类型的最佳接种密度。
γ. 血清浓度
在培养基中添加血清可能对血管生成过程产生影响,其中多数情况下,血清具有抑制血管形成的作用。为了探究最佳的血清浓度条件,建议在按照第 α 节和第 β 节所述的条件下,测试 0% 至 20% 的不同血清浓度梯度。这一实验设计将有助于确定何种血清浓度最有利于血管的形成和细胞存活。
δ. 放大倍率
放大倍率是决定照相机拍摄视野中孔面积大小的重要参数。由于血管生成过程遍布整个孔的表面区域,因此,需要尽可能提高成像的放大倍率以获取更全面的信息。在不需要详细观测细胞内结构的情况下,推荐使用较低的放大倍率(如 4 倍或 5 倍)。若需深入探究细胞内细节,建议对每个孔进行多次高倍率拍摄,并将所得图像进行拼接处理,以获得更全面的细胞结构信息。
2)设立阳性对照与阴性对照
为建立阳性对照,应选取能够稳定诱导血管生成的培养体系(例如,在含低浓度生长因子的 Matrigel 基质胶和无血清培养基中培养 HUVEC 细胞)。阳性对照旨在验证细胞的健康状态,并确保所观察到的抗血管生成效应归因于目标研究物质。
对于阴性对照的设立,应选用已知能够抑制血管生成的物质(如针对 HUVEC 细胞的舒拉明)。阴性对照用于验证血管生成在细胞中被有效抑制,并为实验结果提供一个基准比较点。
3)实验规划与重复次数
在实验开始之前,需详细计算所需材料的量,包括细胞、培养基、凝胶基质和实验物质,以及实验室设备和空间需求、时间安排等。
为确保统计分析的准确性,建议至少进行 4 次独立的重复实验,每次实验至少包含 8 个重复孔。实验次数应根据数据的一致性和稳定性来确定。严格遵守实验规程对数据的可靠性至关重要。
对数据集进行 T 检验,若p值≤ 0.05*(或p值≤ 0.01**),则表明模型具有充足的统计学意义,可无需进一步增加实验次数。
数据分析
1)图像分析
为了量化血管生成的特征,实验者需对显微图像进行深入分析。这一过程可以通过图像处理软件(例如,ImageJ中的「AngioTool」插件)进行手动操作,或者选择将图像传输至自动图像分析仪(ACAS)进行自动处理。
在血管生成分析中,关键的量化指标包括:
-
细胞覆盖面积(以百分比为单位)
-
血管总长(以像素为单位)
-
分支点总数
-
环总数
在实验流程中,尽管所有关键指标均可能展现出相似的特征,但出于效率和准确性的考虑,我们推荐仅评估其中一个参数。其中,血管总长因其稳定性和可追溯性而被视为最佳选择。因此,我们建议将血管总长作为评估血管生成情况的主要参数。
2)数据处理
每个分析孔产生一个血管长度值,然后将一个实验(每个条件至少 8 个孔)的数值相加,计算出标准偏差,标准偏差应小于 10%——这只是一个实验数据点。为了进行稳定的统计分析,每个条件至少需要四个数据点——请记住,每个数据点由 8 个单孔组成。
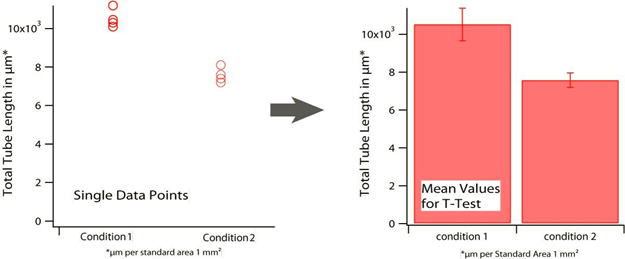
3)数据解读
T 检验是一种统计方法,用于检验两个独立数据集(遵循 t 分布)之间是否存在显著的统计学差异。在进行此检验时,实验的重复次数和样本量均对分析结果具有显著影响。为进行 T 检验,可以使用专业的统计分析软件(如SAS),或 Microsoft Excel 等电子表格软件中的统计功能。
值得注意的是,实验者应充分考虑血管生成数据的实际预测意义。血管生成是一个包含多步生化反应和途径的复杂过程。该实验被广泛应用于物质的筛选和初步预测其抗/促血管生成作用。然而,它并不能直接解释观察到的效果产生的具体机制。为明确这一机制,还需进行更为详尽的生化分析和实验研究。