广州科适特科学仪器有限公司代理商
10 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.3999999999999999
- 1.4
- 0.3999999999999999
- 3.4
IBIDI易必迪划痕实验/伤口愈合3孔插件/培养皿
询价
推荐产品
公司新闻/正文
在 ibidi 3D 细胞培养微插件(micro-Insert 3D)进行由趋化作用驱动的细胞侵袭实验
59 人阅读发布时间:2026-03-23 11:29
前言
理解细胞侵袭对于揭示肿瘤进展和免疫细胞迁移的机制至关重要,此两者均为疾病发展和治疗反应的关键因素。本应用指南描述了在 ibidi 3D 细胞培养微插件(ibidi micro-Insert 3D,80496 或 80499)中进行由趋化作用驱动的细胞侵袭实验(以下简称「细胞趋化-侵袭实验」)的具体方法;插件内填充有 3D 胶原蛋白 I 基质胶,实验者可借此评估 Jurkat T 细胞的迁移行为。
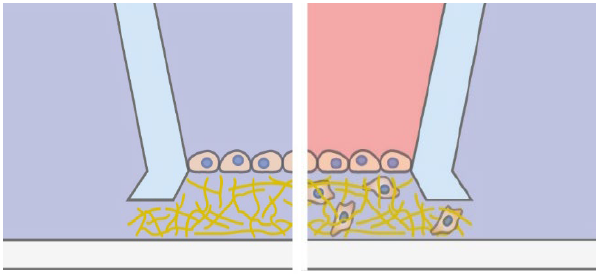 图 1:在 ibidi 3D 细胞培养微插件中进行细胞趋化-侵袭实验。
图 1:在 ibidi 3D 细胞培养微插件中进行细胞趋化-侵袭实验。Jurkat T 细胞是快速迁移淋巴细胞的代表,将其接种在胶原蛋白基质胶顶部表面,并使其暴露于相邻储液池(即 ibidi 3D 细胞培养微插件的内、外孔)中由不同浓度的胎牛血清产生的浓度梯度中,如此培养 24 h 后通过成像和深度量化评估细胞侵入胶原蛋白基质胶的情况。与处于化学均一环境中的细胞相比,暴露于胎牛血清浓度梯度中的细胞侵入得更深,且这一现象与血清的绝对存在与否无关。
该实验模拟了 3D 环境中的趋化-侵袭过程,揭示了方向信号在促进细胞通过细胞外基质成分进行主动迁移中的作用,并为在生理相关条件下研究免疫细胞迁移和肿瘤微环境相互作用提供了一个可靠且可重复的实验平台。
实验材料
1)试剂与缓冲液
-
3D 细胞培养微插件(80499,ibidi)
-
μ-Plate 24 孔培养板,经 ibiTreat 表面处理(82426,ibidi)
-
牛源胶原蛋白 I(50303,ibidi)
-
Jurkat 细胞(ACC 282,德国微生物菌种保藏中心 DSMZ)
-
RPMI 1640 培养基(21875034,Gibco,Thermo Fisher Scientific)
-
胎牛血清(10270106,Gibco,Thermo Fisher Scientific)
-
10× RPMI 1640培养基(R1145,Sigma)
-
1 M NaOH(以超纯水配制)
-
7.5% NaHCO₃(S8761,Sigma)
-
无菌超纯水
2)仪器与设备
-
细胞培养箱(具备加湿功能,温度 37°C,二氧化碳浓度 5%)
-
标准细胞培养设备(无菌操作台、细胞消化试剂盒、培养瓶、配备合适吸头的移液器等)
-
冷却的铝珠或冰块
实验步骤
对于每一次细胞趋化-侵袭实验,需制备 3 种不同样品,且每种样品均需设置 3 个平行重复对照组(如图 2 所示):
-
趋化因子浓度梯度样品(-/+):仅在插件外孔中添加趋化因子(本实验采用 10% 胎牛血清作为趋化因子);
-
趋化因子均匀分布样品(+/+):在插件的外孔、内孔以及基质胶中均添加趋化因子(10% 胎牛血清);
-
无趋化因子样品(-/-):培养基及基质胶中均不添加任何趋化因子。
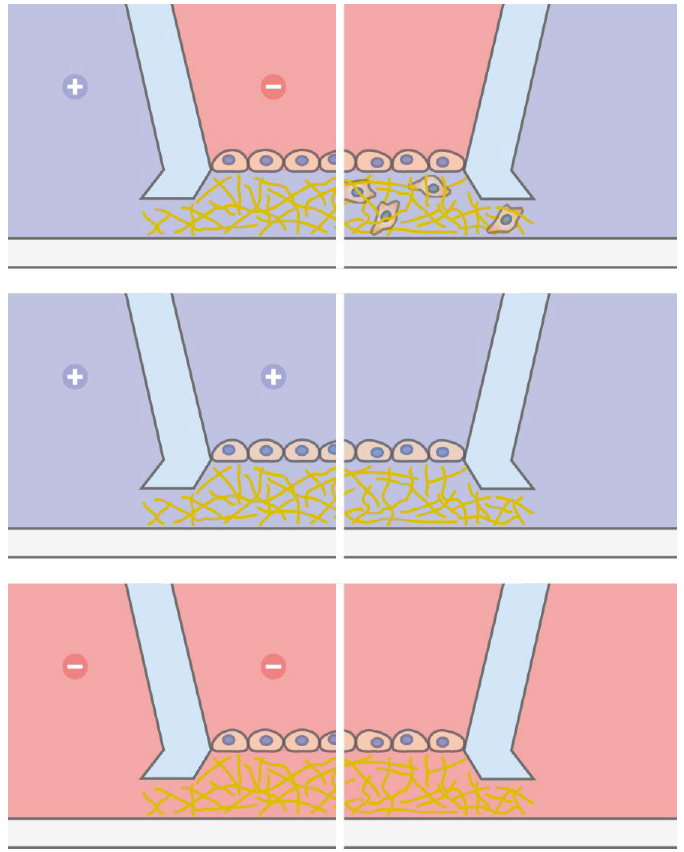 图 2:实验设计。
图 2:实验设计。1)制备样品
-
将 9 个 ibidi 3D 细胞培养微插件(以下简称「插件」)分别放入 μ-Plate 24 孔培养板的孔中;轻轻按压每个插件以排出滞留的气泡并令其与培养板底部紧密接触;
-
在培养板中未放置插件的空孔内加入无菌水或磷酸盐缓冲液,以减少孵育过程中的蒸发;
2)配制胶原蛋白基质胶
开始配制胶原蛋白基质胶前,请先阅读胶原蛋白使用说明书(如下)。本实验需要配制以下 2 种基质胶:
-
无血清基质胶(用于 -/+ 及 -/- 样品);
-
含 10% 胎牛血清基质胶(用于 +/+ 样品)。
重要提醒:配制胶原蛋白基质胶时的移液操作 α. 移取基质胶时务必使用预冷至 4°C 的移液器吸头; β. 由于胶原蛋白基质胶粘度较高,建议在所有操作步骤中采用反向移液法:将移液器按压至第二档位,使吸头完全充满基质胶;释放基质胶时仅按压至第一档位——此方法虽会在吸头内残留少量需弃去的基质胶,但可显著提高移液体积的准确性;实验者亦可选用专为高粘度溶液设计的移液器吸头,如 Eppendorf Visco Tips 或 Gilson Microman E 等; γ. 需特别注意,即使处于 4°C 环境,配制完毕的基质胶在部分凝固前仅可保存 5 min,请严格控制操作时间。
-
根据表 1 配制基质胶(1.5 mg/mL 牛源胶原蛋白,含或不含 10% 胎牛血清);按表 1 所列顺序依次加入各组分,并在冰上用移液器充分吹打混匀以延缓凝胶化进程;
-
在每个插件的内孔中加入 20 μL 上述基质胶;为保证基质胶层平整,移液时移液器吸头需垂直对准孔中心;
-
盖上培养板盖子,将培养板置于培养箱中静置约 30 min,待基质胶聚合。
温馨提示:若需更改基质胶配方,实验者可使用 ibidi Collagen Calculator 计算胶原蛋白基质胶体系中各组分的用量:表1:含或不含胎牛血清的 300 μL 1.5 mg/mL 胶原蛋白基质胶移液方案。
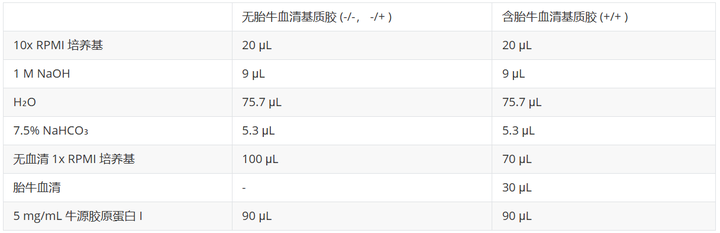 表1:含或不含胎牛血清的 300 μL 1.5 mg/mL 胶原蛋白基质胶移液方案。
表1:含或不含胎牛血清的 300 μL 1.5 mg/mL 胶原蛋白基质胶移液方案。3)接种细胞
-
在基质胶聚合期间,按常规方法收集 Jurkat 细胞,并分别用无血清培养基、含 10% 胎牛血清培养基重悬细胞并调整细胞密度至 3×105cells/mL">3×105cells/mL(前者用于 -/- 及 -/+ 样品,而后者用于 +/+ 样品);
-
从培养箱中取出培养板,在显微镜下确认基质胶聚合状态;若基质胶仍未完全聚合,需继续孵育10~15 min;
-
在每个插件的外孔中加入 250 μL 培养基,其中 -/- 样品加入无血清培养基,而 -/+ 及 +/+ 样品加入含 10% 胎牛血清的培养基;
-
在每孔内的基质胶表面滴加 25 μL 相应细胞悬液,注意避免移液器吸头接触基质胶;
-
盖上培养板盖子并放回培养箱,令细胞侵袭基质胶 24 h;
4)镜检成像
-
24 h 后,用相差显微镜镜检 Jurkat 细胞在基质胶中的侵袭情况;
-
对于每个插件,在插件中部随机选取3 个基质胶层平整的 XY 位置,并在每个位置采集 Z 轴序列图像——由基质胶顶部(多数细胞聚焦层面)开始,以 13 μm 为步长向下扫描至孔底。
请注意!相邻图像间的 Z 轴间隔应近似等于单个细胞的直径(约 8~15 μm),以确保最终图像序列中能完整捕获所有细胞。
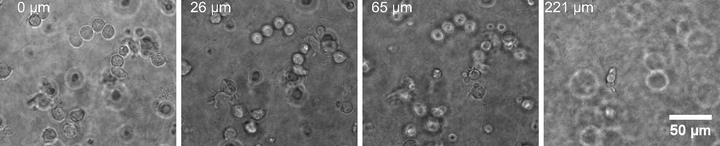 图 3:在胎牛血清浓度梯度(-/+)作用下 Jurkat 细胞侵袭基质胶 24 h 后的 Z 轴序列图像典例。
图 3:在胎牛血清浓度梯度(-/+)作用下 Jurkat 细胞侵袭基质胶 24 h 后的 Z 轴序列图像典例。该序列图像系相差显微镜在插件的同一位置不同 Z 轴平面采集而得。首张图像(0 μm)显示位于基质胶表面的细胞,后续图像仅聚焦于已侵袭至对应深度的细胞。图像由配备 40× LD Plan-Neofluar 物镜的蔡司 Axio Observer Z1 显微镜采集。
数据分析与实验结果
为评估细胞对趋化因子胎牛血清所做出的侵袭能力,需针对每个孔计算深度评分,该评分依据单个 Z 平面图像中处于聚焦状态的细胞数量,来反映细胞向基质内侵袭的深度。
侵袭指数(Invasion index)的计算方法为:将每个深度 h(单位:μm)处处于聚焦状态的细胞数量(nₕ)之和,乘以对应的深度 h,再除以所有深度处的细胞总数(N),即:
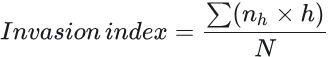
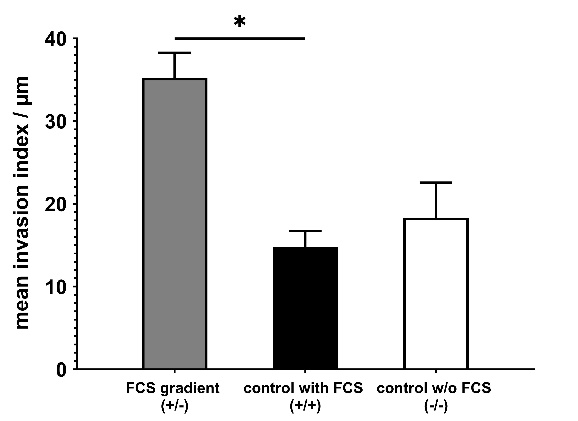 图 4:在胎牛血清浓度梯度驱动下 Jurkat 细胞的趋化-侵袭情况。
图 4:在胎牛血清浓度梯度驱动下 Jurkat 细胞的趋化-侵袭情况。图 4 所示数据为实验开始 24 h 后各组之平均侵袭指数(平均值±标准误,n= 2 次独立实验,每次实验均设 3 个平行重复对照组)。与处于均一胎牛血清浓度样品中的细胞相比,暴露于胎牛血清浓度梯度环境中的细胞向胶原蛋白基质胶内侵袭的深度显著更深。请注意:在此示例中,若细胞跨越多个切片,仅在其细胞中心平面所在切片处于聚焦状态时计数 1 次。
结语
运用 ibidi 3D 细胞培养微插件开展细胞趋化-侵袭实验,此方法为量化免疫细胞于 3D 胶原蛋白基质中的迁移情况提供了一种可靠且契合生理状态的研究手段。在不同血清条件下所观测到的细胞侵袭深度差异,彰显了方向信号在调控细胞运动能力方面的关键作用。该实验方案在细胞趋化迁移行为的对比研究中极具适用性,同时可根据研究需求进行调整,以适配其他细胞类型或趋化因子,进而深入探究细胞侵袭与微环境相互作用的多维度特性。