广州科适特科学仪器有限公司代理商
10 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.5
- 1.5
- 0.5
- 3.5
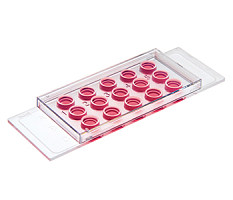
µ-Slides With Single-Cell µ-Pattern(单细胞µ-模式的µ-Slides载玻片)-货号83801
询价
推荐产品
公司新闻/正文
μ-Pattern 细胞培养微区块初探
34 人阅读发布时间:2026-03-20 10:36
前言
即便在相同的培养条件下,细胞也极少表现出完全相同的行为。在常规培养皿中,有些细胞会「躺平」而向四周铺展,而另一些则会「抱团」而形成紧凑形态;有些细胞会极化并迁移,而另一些则在原地分裂。细胞形态、黏附面积以及局部胞间连接的差异,会直接导致信号传导、迁移速度、分化潜能、药物反应,甚至细胞存活和命运等方面的不同 。人们常将此归因于生物异质性——虽然其中部分原因确实如此,但另一部分则仅仅是空间随机性导致的。
μ-Patterning 微区块技术则从根源上解决了这一问题。
在本文中,笔者将一一阐述 μ-Patterning 微区块技术的发展历程、不同形状 μ-Pattern 微区块在研究中的应用以及空间约束在现代细胞生物学研究中日益重要的原因。
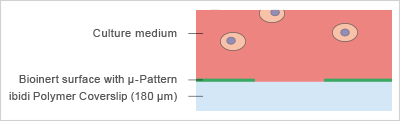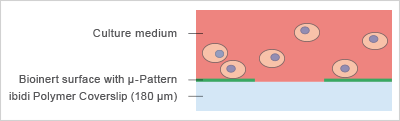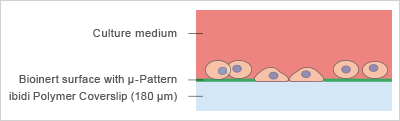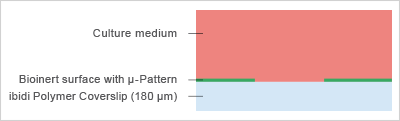 图 1:细胞在 μ-Pattern 微区块表面上的行为。
图 1:细胞在 μ-Pattern 微区块表面上的行为。μ-Pattern 微区块可以是圆形、方形、线形,也可以根据需求定制设计,且尺寸均以 μm 为单位。通过调整 μ-Pattern 微区块的大小及间距,实验者即可控制每个 μ-Pattern 微区块上的细胞数量、相邻细胞之间的距离,以及细胞是保持独立状态还是聚集形成细胞团簇。此时,几何形状成为了一个固定的实验参数,而非不可控变量,这一理念一直是细胞形态发生和细胞骨架组织研究领域的核心 。
随着时间的推移,这一理念发展显著。早期的方法是利用弹性体模具将细胞外基质蛋白压印至培养表面上——此方法效果显著,但需要专业的技术知识和精心的迭代优化。表面化学领域的进步改善了背景钝化效果和 μ-Pattern 微区块稳定性,使针对细胞的空间限制更加可靠。如今,现成的 μ-Pattern 微区块化基底省去了制备步骤,提供了无菌且成像效果卓越的平台,让任何细胞生物学实验室都能轻松实现针对细胞的空间约束,而近期的发展更是进一步提升了其灵活性和工程精度 。
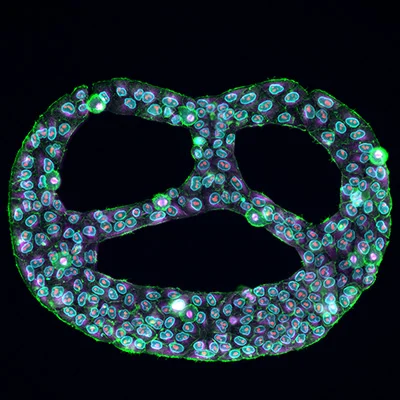 图 2:培养于 μ-Pattern 微区块表面上、经多重免疫荧光染色的 HeLa 细胞。
图 2:培养于 μ-Pattern 微区块表面上、经多重免疫荧光染色的 HeLa 细胞。μ-Pattern 微区块的几何形状为何重要?
μ-Patterning 微区块技术的真正优势在于,它能够在避免实验流程复杂化的前提下实现标准化的细胞空间约束。通过选择 μ-Pattern 微区块的几何形状,实验者即可设计不同的实验,以解决不同的生物学问题。
1)单细胞阵列
μ-Pattern 微区块表面具有明确间距的小面积黏附区域,能让单个细胞彼此独立地附着。这种设置在基于成像的检测中特别有用,因为细胞重叠会使图像分割和定量分析变得复杂。有序排列的单细胞阵列可提高图像清晰度,并使自动化分析更加可靠。对于依赖精确形态测量或荧光强度分析的研究而言,仅空间分离这一项就能显著提高数据质量。
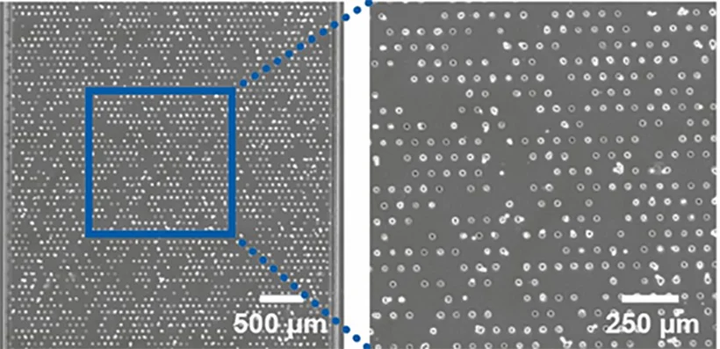 图 3:培养于经层粘连蛋白包被的 μ-Pattern 微区块表面(µ-Slide VI 0.4 µ-Pattern ibiTreat, sqr30, pit75, hex)上的 A549 细胞。
图 3:培养于经层粘连蛋白包被的 μ-Pattern 微区块表面(µ-Slide VI 0.4 µ-Pattern ibiTreat, sqr30, pit75, hex)上的 A549 细胞。2)多细胞阵列
较大的黏附区域可让多个细胞黏附于一个特定区域内。由于其周围的生物惰性表面可防止不合预期的细胞黏附,细胞仅会在 μ-Pattern 微区块内聚集,形成可重复的微群落。在胞间通讯研究、肿瘤微环境模型构建以及免疫细胞互作检测中,这种受控的细胞聚集现象极具价值。在这些研究中,一致的细胞空间排列简化了不同实验间的对比分析。甚至有研究利用具备特定几何形状的细胞群落在体外复现了早期胚胎的空间组织结构 ,这表明仅几何形状本身就能对细胞的群体行为产生影响。
 图 4:固定在多细胞阵列(µ-Slide VI 0.4 µ-Pattern ibiTreat, cir200, pit600, hex)上的 RCC-26 细胞;在大鼠尾源胶原蛋白 I 基质胶中加入效应 T 细胞即可诱导 RCC-26 细胞形成凋亡小体。
图 4:固定在多细胞阵列(µ-Slide VI 0.4 µ-Pattern ibiTreat, cir200, pit600, hex)上的 RCC-26 细胞;在大鼠尾源胶原蛋白 I 基质胶中加入效应 T 细胞即可诱导 RCC-26 细胞形成凋亡小体。3)细胞球状体生成
μ-Patterning 微区块技术还能助力实现细胞球状体(spheroid)的可控生成。当将处于悬浮状态的细胞接种至由完全非黏附背景环绕的特定黏附位点(即 μ-Pattern 微区块)上时,细胞会形成结构紧凑、大小均匀的聚集体。此法减少了不同细胞球状体之间的差异,提高了药物筛选及药物试验的可重复性。实验者无需面对大小各异的异质性细胞聚集体,而是可以研究标准化的 3D 细胞结构——这一理念与基质调控的类器官系统类似 。
4)线形阵列
线形 μ-Pattern 微区块阵列可营造微通道环境,引导细胞定向排列和定向生长。细胞会沿着线条的几何形状排列,这对于研究神经突延伸、细胞骨架组织或结构化迁移大有用处。研究表明,与无约束的 2D 培养相比,一维空间限制能够更好地模拟体内纤维状迁移 。除此之外,线形 μ-Pattern 微区块阵列可减少细胞的随机排列现象,从而令定向过程和细胞内运输的分析更加一致,也更为简便。

图 5:培养于线形经层粘连蛋白包被的 μ-Pattern 微区块阵列上的 HT-1080 细胞。
敬请注意:在上述 μ-Pattern 微区块形式中,μ-Patterning 微区块技术本身并不会改变细胞的生物学特性,它仅仅消除了可能干扰实验结果解读的不可控空间差异。
μ-Pattern 微区块与细胞灌流培养
体内细胞很少处于静态环境之中;恰恰相反,组织会持续受到流体运动、营养梯度和机械力的作用。μ-Pattern 微区块技术可与灌流培养系统(如 ibidi 流体剪切力系统)相结合,将上述动态条件引入受控的体外实验之中。
当在通道载玻片中灌流培养已 μ-Pattern 微区块化的细胞或细胞聚集体时,持续循环的培养基可提供稳定的营养供应以及明确的剪切应力。在灌流条件下维持的结构化细胞球状体可表现出更更好的紧密性和长期稳定性,而贴壁细胞则能在保持其空间排列的同时受到机械刺激。将几何约束与流体动力学相结合,研究人员即可在更贴近生理状态的环境中探究空间排列与机械信号的互作机制。此举令 μ-Pattern 微区块技术突破了静态约束的局限,更趋近于模拟组织真实环境的实验条件。
定制 μ-Pattern 微区块
细胞如此多姿,并非所有的生物学问题都能借助既有规格的 μ-Pattern 微区块迎刃而解。不同的实验设计可能需要特定的空间排列、分隔的互作区域或独特的尺寸,而上述种种并非常规规格所能提供。定制 μ-Pattern 微区块令实验者能够围绕其科学问题设计 μ-Pattern 微区块的几何形状。无论实验者的目的是创建分区共培养系统、结构化细胞网络还是设定相互作用界面,定制都能保证 μ-Pattern 微区块的空间排列与研究目的相符。

图 6:定制 μ-Pattern 微区块。
由此观之,μ-Patterning 微区块技术已不仅仅是一种控制细胞黏附的手段,它已成为实验设计的一部分。研究人员可根据检测需求定制几何形状,将空间约束直接融入研究逻辑中,而非令实验去适应固定的模式。
展望
现代细胞生物学高度依赖成像技术、定量分析以及实验结果的可重复性。标准化的细胞空间约束对于高内涵分析、基于人工智能的图像处理以及空间组学研究大有益处。μ-Pattern 微区块技术可减少空间干扰,提高不同培养孔、不同时间点以及不同实验室之间实验结果的可比性。
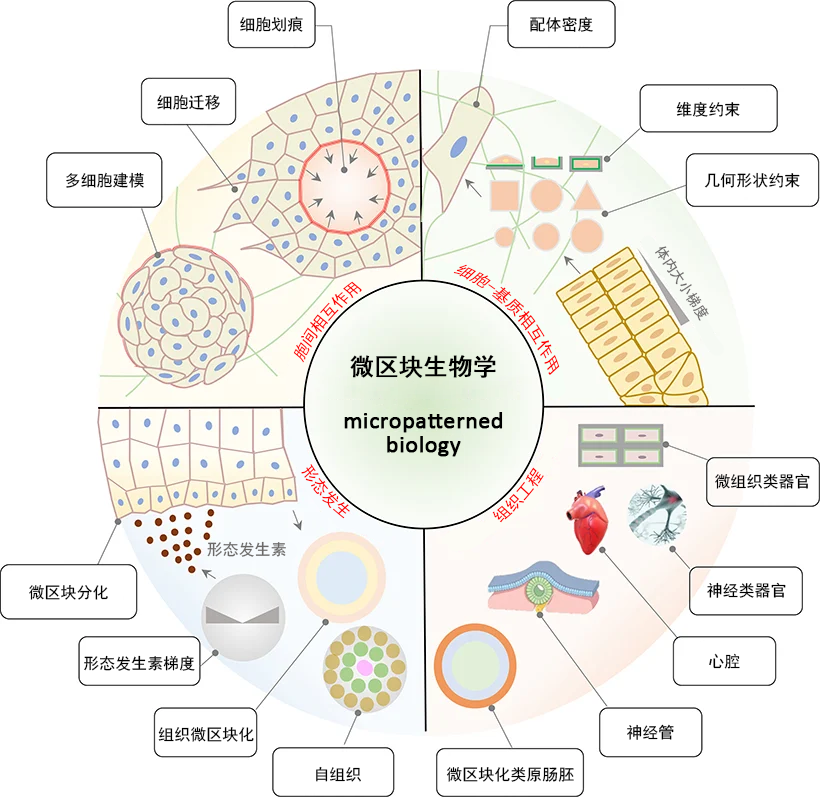
图 6:微区块生物学(micropatterned biology)的应用范围。
在免疫学领域,明确界定的靶细胞阵列简化了活细胞相互作用检测流程;在毒理学与药物研发领域,均一的细胞球状体阵列有助于实现可重复的筛选工作流程;在神经科学领域,引导性微通道能够清晰呈现细胞定向生长模式。总而言之,在上述各个学科领域中,空间约束均使科学的视野更加清晰。
随着实验系统日趋复杂,在微米尺度上控制几何形状或将变得更为重要。最初仅用于约束细胞黏附位置的 μ-Patterning 微区块技术,现已发展为一种创新性实验设计方法。如今,μ-Patterning 微区块技术将赋予科学家精准且富有创意地设计实验架构的能力。
「天下大事,必作于细。」有时,更为明晰的生物学见解,源于对微米尺度精准调控的有效实现。