广州科适特科学仪器有限公司代理商
10 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.3999999999999999
- 1.4
- 0.3999999999999999
- 3.4
CoolLED pE-400 可控白光
询价
推荐产品
公司新闻/正文
「走」为上策:细胞迁移中的「生」与「病」
219 人阅读发布时间:2025-04-22 14:30
前言
试想一下,你膝盖受了伤,几乎是一瞬间,你的身体便开始动员起来。皮肤细胞迁移至伤口处以愈合伤口,免疫细胞迅速涌入以对抗感染,血管亦重新排列以恢复血液循环。从胚胎发育的最初阶段到受损组织的再生,细胞迁移都是塑造生命本身的基本过程。
细胞们并非盲动的乌合之众——它们遵循精确的信号,以惊人的精确度在组织中穿行。这种迁移能力是关键生物学功能的基础,包括器官形成、伤口愈合以及抵御感染。然而,当这一套受到严格调控的机制遭到破坏时,就可能导致慢性炎症、自身免疫性疾病甚至癌症等疾病 。
那么,细胞是如何知晓何去何从的呢?它们又是如何移动的呢?科学家们又该如何研究和操控这些机制,以更好地理解健康和疾病呢?让我们一同探索细胞迁移这一奇妙的世界吧。
细胞为何移动及如何移动
细胞虽不会行走,但它们拥有复杂的内部骨架,得以伸展和收缩,从而在组织中移动前行。细胞的移动并非随机,而是高度协调的,并受到外部信号和内部信号级联反应的调控。大致而言,细胞通过不同机制实现迁移(如图 1 所示) :
-
阿米巴样迁移(Amoeboid Migration):细胞通过伸出突起(如伪足)向前推进,并挤过间隙,其移动方式与阿米巴原虫相似;
-
间充质样迁移(Mesenchymal Migration):细胞附着于周围结构,并借助富含肌动蛋白的突起(称为片状伪足和丝状伪足)拉动自身向前移动;
-
集体迁移(Collective Migration):细胞群体作为一个协调的单元共同移动,这在伤口愈合和胚胎发育等过程中至关重要。
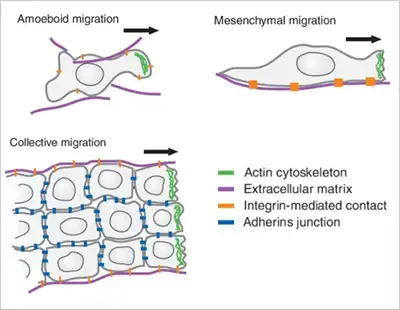
图 1
正道:发育与愈合过程中的细胞迁移
自生命最初阶段起,细胞便处于移动状态。在胚胎发育过程中,神经嵴细胞会进行长距离迁移,进而形成心脏、骨骼和神经系统等结构。若迁移不精确,便可能导致出生缺陷和发育障碍。这一高度协调的过程可确保器官和组织在正确的时间出现在正确的位置,塑造身体的结构与功能 。
在生命后期,细胞迁移在伤口愈合与组织再生过程中发挥着核心作用。当组织受损时,角质形成细胞、成纤维细胞和免疫细胞会协同工作以修复损伤。成纤维细胞迁移至伤口处,沉积胶原蛋白以形成新组织,而内皮细胞则通过血管生成形成新的血管,恢复氧气和营养供应 。在化学趋化作用的引导下,免疫细胞迅速涌向损伤部位以对抗感染、清除碎片并调节炎症反应 。这种错综复杂的细胞协调可确保高效愈合,并防止出现慢性伤口或过度瘢痕。
通过研究发育与愈合过程中的细胞迁移,科学家能够更好地理解细胞如何感知周围环境、响应信号并协调自身移动。活细胞成像技术使研究人员能够观察这些微小「旅行者」的活动,捕捉细胞如何推动、牵拉和协作以构建组织并修复损伤。这些见解不仅揭示了有序迁移之美,还揭示了当这种调控机制失效时会发生什么。虽然精确迁移对于构建器官和愈合伤口至关重要,但细胞的移动能力也可能走向歧途——助长癌症等疾病的发生,此时异常细胞会挣脱束缚并侵入新的区域。
歧途:癌症转移与失控的细胞迁移
虽然受控的细胞迁移对生命活动至关重要,但细胞的移动能力也可能引发致命疾病。癌症最令人恐惧的一个方面便是转移,即肿瘤细胞脱离原发部位,经血液或淋巴系统转移,并在远处器官中形成继发性肿瘤 。癌细胞盗用许多正常细胞所采用的机制,从而导致一系列危险后果 (如图 2 所示):
-
癌细胞通常会经历上皮 - 间质转化(EMT),这使其能够脱离原发肿瘤,并增强其迁移能力;
-
一旦癌细胞具备迁移能力,便会无视常规的迁移终止信号,并突破组织屏障;
-
为了促进自身转移,癌细胞会劫持血管生成(即形成新血管的过程),这些新血管为癌细胞在体内的迁移提供了直接通道,使它们能够进入远处器官,在那里形成继发性肿瘤并进一步推动疾病进展。
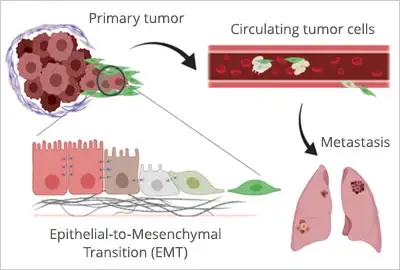
图 2
细胞迁移与癌症以外的疾病
尽管癌症转移是失控迁移最臭名昭著的例子,但异常细胞移动也与其他疾病相关:
-
炎症性疾病:在类风湿性关节炎和哮喘等疾病中,免疫细胞过度迁移,导致慢性炎症和组织损伤。
-
神经退行性疾病:发育过程中神经元的异常迁移与癫痫和精神分裂症等疾病存在关联 。
-
纤维化病变:当成纤维细胞迁移过于活跃时,会在肺部(肺纤维化)或肝脏(肝硬化)等器官中形成过多的瘢痕组织,进而损害器官功能 。
如何研究细胞迁移
研究细胞迁移对于理解关键生物过程(包括组织修复、免疫反应以及癌症转移)至关重要。然而,传统的迁移实验方法在可重复性、生理相关性以及实时观测等方面常常面临挑战。研究人员不断改进方法,以克服这些局限,从而更深入地了解细胞运动机制。
细胞划痕实验
细胞划痕实验用于研究细胞如何迁移以愈合划痕,从而模拟体内的组织修复过程。该技术广泛应用于再生、纤维化以及肿瘤细胞迁移方面的研究。然而,划痕大小和形状的不一致可能导致结果存在差异,且机械划痕(如利用划痕针或移液器吸头进行划痕)可能会影响细胞行为。采用明确的无细胞划痕代替人工划痕,有助于确保细胞划痕实验更具可重复性和可量化性。
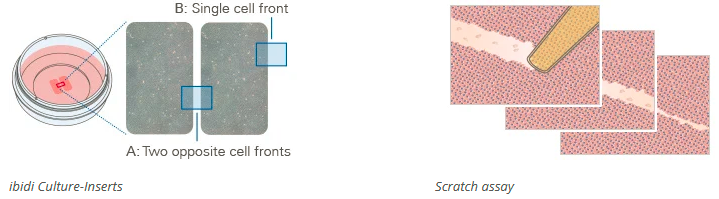
图 3
针对如此痛点,ibidi 祭出了细胞划痕神器——ibidi 细胞划痕插件(ibidi Culture-inserts,81176)。与传统划痕实验不同,ibidi 细胞划痕插件(ibidi Culture-inserts)可创建精确、无游离细胞或细胞碎片的划痕(如图 2 所示)。这使得不同的细胞划痕实验具有出色的可重复性,并可进行精确比较。
细胞趋化实验
细胞趋化实验用于研究细胞如何响应化学梯度而移动,该实验在免疫反应、胚胎发育以及癌症转移过程中起着至关重要的作用。传统的 Boyden 细胞趋化腔室(Boyden chamber)缺乏实时可视化功能,仅能对终点测量结果进行分析,且对迁移模式的了解有限。
而 ibidi μ-Slide 细胞趋化载玻片(ibidi μ-Slide Chemotaxis,80326,见图 4)可在 2D 和 3D 环境下进行实时趋化性测量,使研究人员能够在受控梯度条件下对细胞移动进行细致观察。这使得研究人员能够持续追踪迁移动态,对定向移动和细胞行为进行更准确、更定量的分析。
图 4
血管出芽及细胞侵袭实验
血管出芽及细胞侵袭实验用于研究细胞如何侵袭周围组织,这是血管生成、癌症转移以及组织重塑过程中的关键环节。在血管出芽实验中,内皮细胞形成新的毛细血管样结构,从而模拟血管形成过程。在细胞侵袭实验中,癌细胞或基质细胞迁移至 3D 基质胶中,从而模拟肿瘤浸润过程。传统方法往往依赖于复杂的共培养系统或人工支架,而这些方法可能无法完全模拟生理条件。
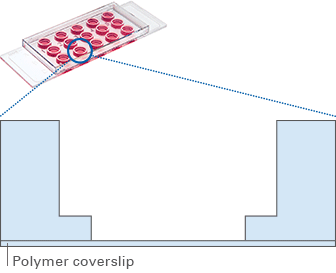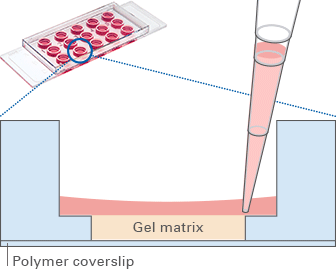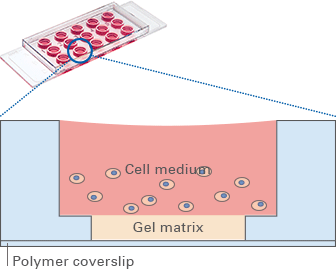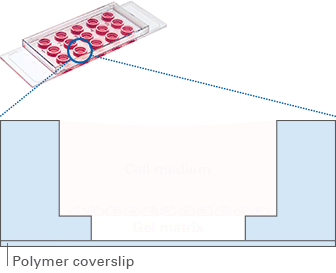 图 5
图 5对此,ibidi 的解决方案是:ibidi µ-Slide 血管生成载玻片(ibidi,81506,见图 5)和 ibidi 3D 细胞培养微插件(ibidi,80496 或 80499,见图 6)。两者为在特定条件下研究血管出芽与细胞侵袭提供了可控环境,同时支持高分辨率成像,使研究人员能够在更符合生理条件的设置中分析血管生成和肿瘤细胞侵袭的动态过程。
跨膜迁移实验
跨膜迁移实验常用于研究细胞如何穿过多孔膜,从而模拟如血脑屏障或内皮层等组织屏障。该实验广泛应用于癌症研究、免疫学及药物测试领域。尽管传统的跨膜迁移实验在研究细胞迁移方面行之有效,但由于其通常采用的人工膜无法完全模拟细胞外基质或组织结构,因此可能无法完全复现体内原生条件的复杂性。此外,这些实验可能会限制显微镜的使用和可视化效果,从而阻碍对细胞行为的实时观察(如图 6 所示)。
对此,ibidi 的解决方案是:ibidi 3D 细胞培养微插件——它提供了一种更贴合实际且更易操作的替代方案,无需使用人工膜即可提供天然的 3D 环境,便于显微镜镜检,并能在更接近原生组织的条件下观测细胞的侵袭与迁移情况(如图 6 所示)。
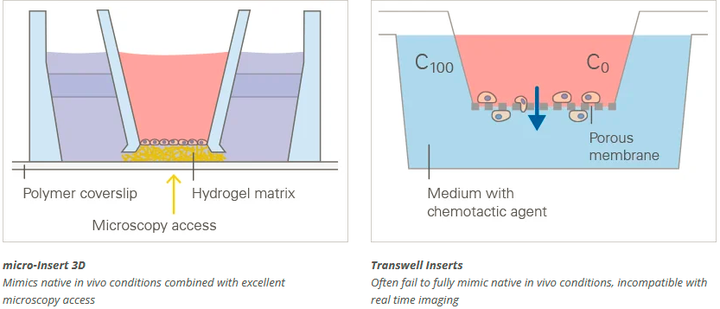 图 6
图 6微流控实验
微流控系统使研究人员能够研究流体流动和剪切应力如何影响细胞迁移——这些因素在血管生物学、转移以及组织工程中发挥着至关重要的作用。传统的静态培养条件无法复现这些动态环境,从而限制了迁移研究的生理相关性。整合了可控流动条件的实验装置有助于研究人员分析剪切应力和组织间液流动如何影响细胞运动和黏附。
对此,ibidi 的解决方案是:ibidi µ-Slide I Luer 3D 通道载玻片(ibidi,87176)。这款载玻片可与 ibidi 流体剪切力系统(ibidi pump system)联用,从而对跨膜迁移进行可控研究。实验者可在载玻片的内腔侧培养内皮细胞,在基底侧培养癌细胞以模拟体内条件,并可施加剪切应力以进行细胞灌流培养。
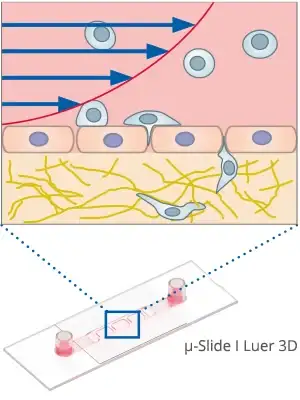 图 7
图 7结语:细胞迁移研究的未来进展
细胞迁移是生物学中最基本却又最为复杂的过程之一。它决定了我们的发育方式、愈合机制,以及相关疾病的发展进程。通过研究这一错综复杂的过程,研究人员能够为从伤口愈合到癌症治疗等各个方面找到新的治疗方法。
如今,借助尖端工具,如先进的活细胞成像技术、微区块化(micropatterned)环境 以及微流控系统,科研人员能够高精度地观察并操控细胞迁移。这些技术正为未来的发现铺平道路,或许有一天,这些发现将帮助我们阻止癌症的扩散、加速组织再生,并更好地理解细胞层面的生命奥秘。
随着我们不断探索细胞迁移之谜,有一点愈发清晰:理解迁移过程并不仅仅是观察细胞的移动——更是揭开生命本身的奥秘。