广州科适特科学仪器有限公司代理商
10 年
手机商铺
- NaN
- 0.3999999999999999
- 1.4
- 0.3999999999999999
- 3.4
推荐产品
公司新闻/正文
使用 ibidi 流体剪切力系统培养内皮细胞实验方法汇总
3952 人阅读发布时间:2020-11-18 17:03
产品正在试用中,戳此申请☛ibidi 易必迪活细胞流体剪切力系统
1、介绍
以下应用描述了将 ibidi 泵系统与 μ-Slide I 0.6 Luer 相结合的实验方案。此外,您将找到一些使用人脐静脉内皮细胞(HUVECs)的建议。该说明可根据您的特定实验需求进行调整。
对于实验,您需要以下材料:
1. µ-Slide I 0.6 Luer, ibiTreat(ibidi80186)
2. ibidi 泵系统
3. 灌注套装红色,15 厘米,内径 1.6 毫米(ibidi#10962)
4. 软管夹
5. HUVECs 与内皮细胞生长培养基
6. 标准细胞培养设备(无菌工作台,细胞分离试剂盒,培养瓶等)
7. 滑动架(IBIDI,80003)
2、培养细胞
根据您的实验方案培养您的细胞。对于 HUVECs,我们推荐补充有 2% 胎牛血清(FCS)的内皮细胞生长培养基(PromoCell,Germany,C-22010)。
注意:内皮细胞不应该长到 100% 的密度。汇合的细胞层进入生长抑制状态,其停止细胞增殖并改变细胞的生理学。
同样重要的是,所有细胞都必须合适。损耗的细胞可能无法承受剪切应力,并会从表面冲洗掉。如果您正在使用原始细胞,那么从一个批次到另一个批次的适应性可能会有很大差异。
3、材料的制备
◆ 开始实验的前一天:
在开始实验前一天,将通道载玻片和流体单元放入培养箱中。将所需量的培养基加入无菌管中,并将其放入培养箱中。将盖子稍微拧开以使管中的过大压力逸出。
将 ibidi 泵系统安装在培养箱旁边,并安排与计算机的连接以及引入培养箱的电缆和管道。将干燥瓶安装在泵的后端口和通向培养箱的管道之间,以便吸入气体环境平衡所有需要的材料,如载玻片,培养基和管道(灌注装置),在 37 °C 和 5% CO2 的培养箱内过夜。这对于防止气泡随时间出现至关重要。
介质在 37 °C 时的粘度约为 0.007 dyn*s/cm2

◆ 实验当天:
按照 ibidi 泵系统说明中的说明将灌注装置安装到流体装置上,然后在储液器中加入约 12 ml 平衡液体(每侧 6 ml)。要从管中去除气泡,请启动中等流量循环。为此,可以在泵控制软件中加载预定义的设置。转到菜单项「Tutorial」,然后选择「加载演示设置」「去除气泡」。
在运行程序时,用手指轻轻敲击管子和适配器以去除气泡。在从管中取出所有空气后,两个储存器的水平应重新平衡至 5 ml。
将载玻片调整到流体单元之前,必须清除所有气泡!系统中剩余的任何气体都会影响流速,在最坏的情况下,会阻止流动或冲洗细胞。
必须在每个新安装的灌注装置上进行此测试,以检查管道的正确插入以清晰可见的流量运行泵(例如「去除气泡」)。夹住灌注装置下环(夹管阀下方)的管道。正确的夹紧位置如图 1 所示

图 1:执行夹点测试以检查管道是否正确:一旦用夹子堵塞管道,就不会观察到从一个储液器到另一个储液器的液体流动。
在两个切换位置进行此测试至关重要!
如果流量没有停止,检查夹管阀中的管道插入:通过拉伸管道并上下移动来调整。然后再次执行夹点测试。
4、流量校准
预测正确的剪切应力或剪切速率,请在开始使用细胞之前测量实验装置的流速。由于温度波动或制造公差等因素,流量值可能与软件程序计算的值不同。请在 PumpControl 说明中找到有关重新校准的详细说明。
在校准流速后,让泵在中压循环(例如,「移除气泡」演示设置)中运行,同时准备载玻片中的细胞。
5、将细胞接种到通道载玻片中
以下所有步骤在无菌工作条件下进行!打开 μ-Slide 的包装并将其放在 μ-Slide Rack 上,然后在准备细胞悬浮液时将盖子放在 Luer 适配器上。为了获得 1×105 cells/cm2 的细胞数,制备 1.6×106 cells/ml 的悬浮液。这总共 2.5 x 105 cells/μ-Slide。通过将移液管尖端直接放在通道的入口上,将 150 μl 细胞悬液填充到通道中。
将盖子放在 Luer 适配器上,在 37 °C 和 5% CO2 下培养 1-2 小时,以实现细胞贴壁。
在此之后,细胞应形成汇合的细胞层,汇合细胞层对于使细胞抵抗剪切应力至关重要。
原则上,细胞现在已准备好连接到灌注装置。如果您没有立即连接,请在储液器中填充一些剩余介质,如下一步所示。
用 60 μl 无细胞培养基填充每个储库。避免将移液管尖端直接指向通道的入口,因为这可能会导致细胞层上的剪切应力不确定。
填充容器后,再次关闭它们,然后在准备流体单元时将细胞放入培养箱中。
如果您想在静态条件下培养细胞超过一天,应至少每 24 小时更换一次培养基!
6、将通道载玻片连接到流体单元装置
细胞贴壁后,您可以将 μ-Slide 连接到流体单元。插入 Luer 适配器时注意不要快速移动,因为这可能会导致细胞的高剪切应力的突然冲动。
停止泵的流动并将带有安装的灌注装置的流体单元放置在层流罩中。
1. 使用塑料夹夹住阀门附近的管子(图 6a)。将 μ-Slide I Luer 放在流体单元旁边。请勿将其直接放在冷金属表面上。使用 μ-Slide Rack 或培养皿防止载玻片冷却。
2. 取下盖子,用新鲜预热的介质清洗通道。缓慢涂抹培养基,以免损伤细胞。
3. 然后用介质填充储液器,直到有一小块液体。
4. 从中间连接器中拉出第一个公鲁尔接头,将其向上拉(图 6-1,b)。确保内部没有气泡。如图 6-1(c-f)所示,将其连接到载玻片上的母鲁尔接口,小心地倾斜。
通过扭转适配器(e),将弯头鲁尔接口连接器紧紧地压入载玻片上的鲁尔适配器
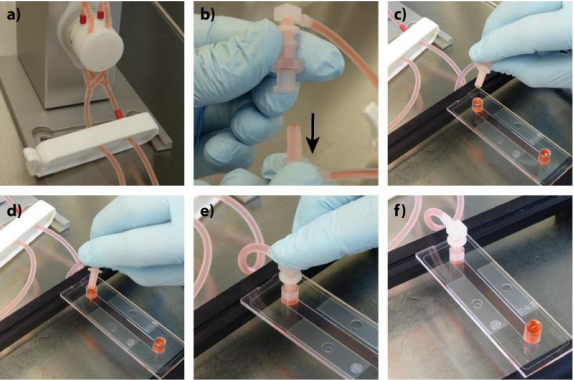
图 6-1:将 μ-Slide 连接到灌注装置(第一个接口)
用第二个鲁尔公适配器重复此过程,然后擦除溢出液体(见图 6-2,g-l)。

图 6-2:将 μ-Slide 连接到灌注装置(第二个接口)
注意尽可能快速,谨慎地工作。细胞将成为任何因素干扰,如果有太多的抖动,可能会分离。连接到管道后,在显微镜下观察细胞!
检查在显微镜下的细胞。至关重要的是细胞层是汇合的,并且当它们暴露于剪切应力时细胞是良好贴壁的。如果细胞从连接过程中受到压力,在开始流动之前给它们几个小时恢复。
将整个组件更换到培养箱中,并将流体单元连接到泵。(气压管和电缆)
7、启动泵
如果实验看起来很好,那么通过使用 ibidi Pump Control 软件打开气压泵来启动流量。
对于此特殊设置,泵控制软件中包含演示文件。转到菜单选项卡「Tutorial」,然后选择「加载演示设置」「演示实验」。
将加载具有中等剪切应力的流动实验的参数。该程序由三个循环组成,这些循环将逐步增加细胞,直到最终剪切应力达到 10 达因/厘米2。

通过切换流体单元的两个阀来维持单向流动。当按照上面的建议施加正压时,流动源将从未标记的管子流到标记的管子(从左到右)。
8、在显微镜上观察细胞
在显微镜上观察细胞,请在储液器中的液位达到平衡时关闭泵。接下来,从气动单元上拆下气压管和电缆。将带有连接的 μ-Slide 的流体单元带到显微镜上,观察细胞。
9、细胞形态学
内皮细胞在其生理环境中暴露于剪切应力。因此,用循环培养基培养细胞将比静态培养中的细胞更接近于它们的通常生理条件。
通过这个实验设置,ibidi 在开始流动实验后的前两天观察到了鹅卵石细胞层的形成。细胞沿流动方向定向。在图 8 和图 9 中,您可以分别比较在流动和静态条件下培养的 HUVECs。除剪切应力外,所有参数都有。
保持不变:细胞处于相同的传代中,并在 μ-Slide I 0.6Luer(ibiTreat)中培养一周。每天更换静态培养基。
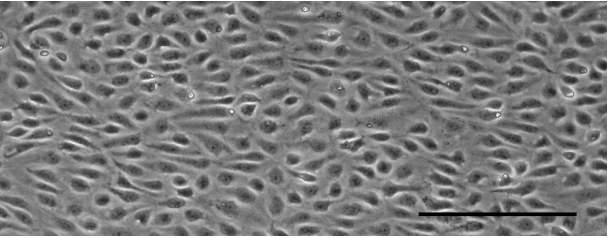
图 8:HUVECs 在 μ-Slide I 0.6 中 20 dyn/cm2 下培养 7 天。细胞在流动方向上显示出良好的取向。比例尺 200 μm。
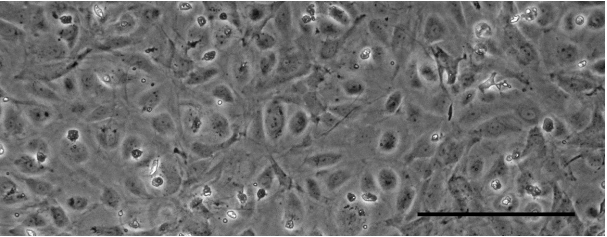
图 9:HUVEC 在 μ-Slide I 0.6 中静态条件下培养 7 天。细胞每天都在变化。比例尺 200 μm。
10、免疫荧光
用标准程序和染色细胞。更换溶液时,首先吸入两个储液器。用 140 μl 新溶液冲洗通道两次。始终从一侧添加新溶液,然后从另一侧吸入。注意通道总是充满液体!
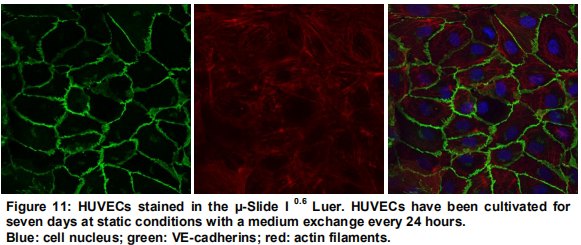
流体实验:下图中的细胞在流动条件下培养。肌动蛋白骨架与流动方向对齐。细胞形状是细长的。

本页显示的细胞在相同的时间段(一周)内在静态条件下培养。VE- 钙粘蛋白清晰可见,但肌动蛋白骨架未排列在应力纤维中,并且细胞不在流动方向上排列。